En continuación con el tema anterior, en el cual abordamos los aspectos clave del tratamiento de agua para calderas de vapor, en esta ocasión detallaremos las consideraciones que se deben tener presentes sobre la dureza del agua en calderas de vapor.
Al agua se le conoce como “dura” o “blanda”. El agua dura contiene impurezas que forman incrustaciones mientras que el agua blanda contiene pocas o ninguna. La diferencia se puede reconocer fácilmente por el efecto del agua en el jabón. Se requiere mucho más jabón para hacer espuma con agua dura que con agua blanda.
La dureza la causa la presencia de sales minerales de calcio y magnesio y son estos mismos minerales los favorecen la formación de incrustaciones. Hay dos clasificaciones comunes de la severidad:
- Dureza alcalina (también conocido como dureza temporal): Bicarbonatos de calcio y magnesio son los responsables de la dureza alcalina. Las sales se disuelven en el agua para formar una solución alcalina. Cuando se aplica calor, se descomponen liberando dióxido de carbono e incrustaciones blandas o lodos. A veces se le conoce como “dureza temporal”, porque la dureza se elimina al hervir. Este efecto se puede ver como incrustaciones en el interior de una hervidora de agua eléctrica. En las siguientes figuras verás este asunto, en la segunda de ellas verás representada la situación dentro de la caldera.
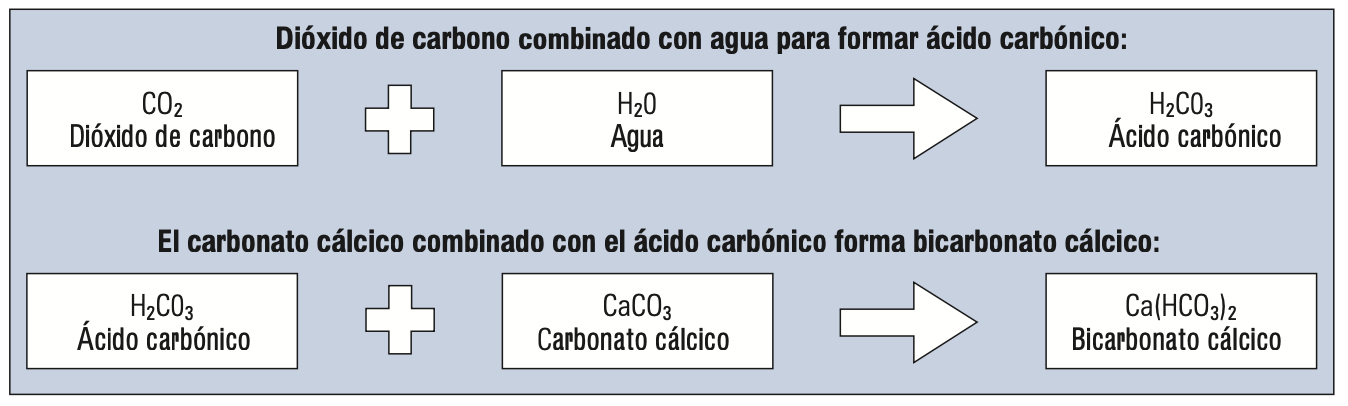
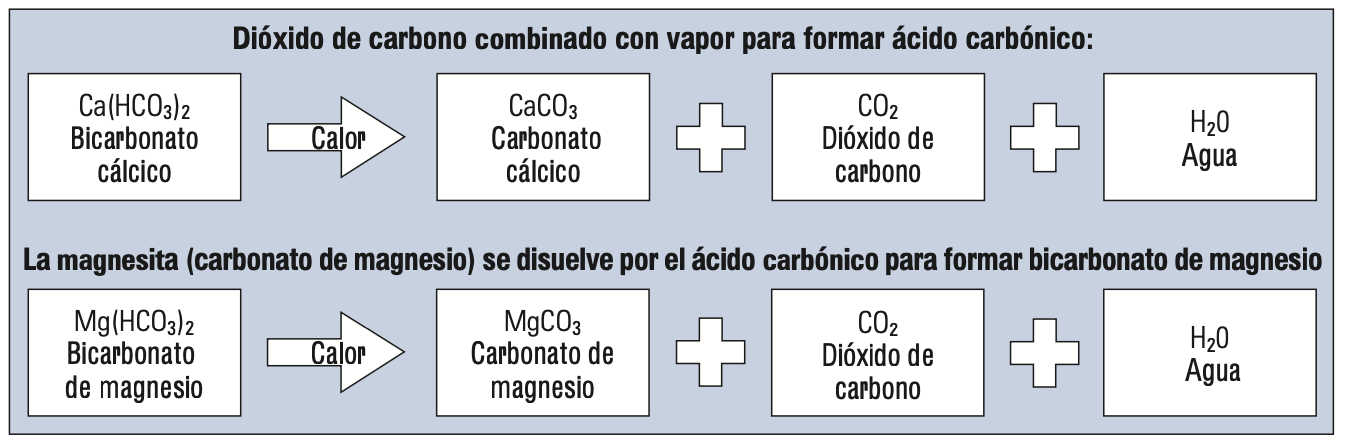
- Dureza no alcalina o carbonatos (también conocido como dureza permanente): También es debida a la presencia de sales de calcio y magnesio en forma de sulfatos y cloruros. Estos se precipitan fuera de la solución, debido a su reducida solubilidad cuando aumenta la temperatura forman incrustaciones duras que son difíciles de eliminar. Además, la presencia de sílice en el agua de caldera también puede producir incrustaciones duras y puede reaccionar con calcio y sales de magnesio para formar silicatos que puede impedir seriamente la transferencia de calor en los tubos de humos y hacer que se recalienten.
Consideraciones acerca de la dureza total del agua en calderas de vapor
La dureza total no se puede clasificar como un tipo de dureza, sino como la suma de las concentraciones de iones de calcio y de magnesio presentes cuando éstos son conocidos como CaC03. Si el agua es alcalina, una parte de esta dureza, igual en magnitud a la alcalinidad total y también conocida como CaC03, se considera como dureza alcalina, y el resto como dureza no alcalina, tal y como se muestra en la siguiente figura:

Sales de sodio que no forman espuma
Sales no duras, como las sales de sodio también están presentes y son mucho más solubles que las sales de calcio o magnesio. Estas no formarán generalmente incrustaciones en las superficies de una caldera, como se ve en la siguiente figura:
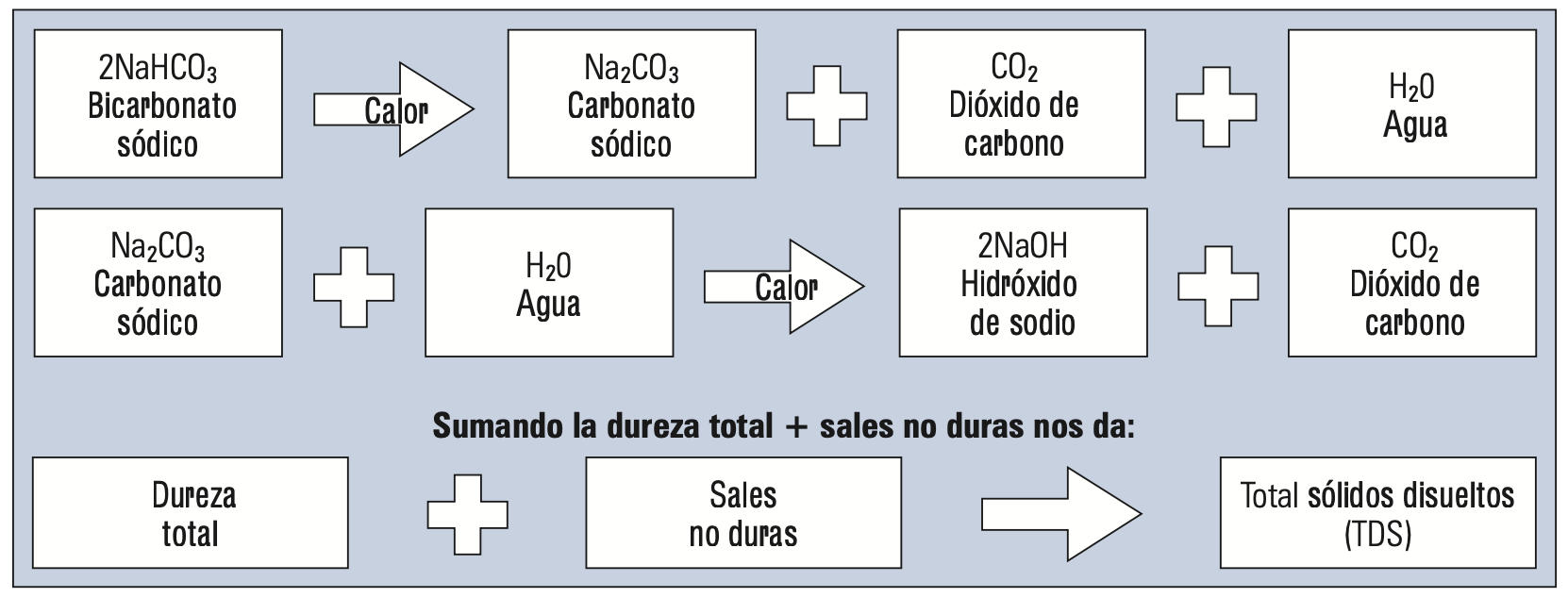
Unidades comparativas
Cuando las sales se disuelven en agua forman partículas con carga eléctrica llamada iones.
Las partes metálicas (calcio, sodio, magnesio) se pueden identificar como cationes porque están atraídos al cátodo y tienen cargas eléctricas positivas.
Los aniones son partes no metálicas y tienen las cargas negativas – bicarbonatos, carbonatos, cloruros, sulfatos, están atraídos hacia el ánodo. Cada impureza se expresa generalmente como la cantidad química equivalente de carbonato de calcio que tiene un peso molecular de 100.
Valor de pH como otro aspecto a tener en cuenta en el tratamiento del agua en calderas de vapor
Otro término que hemos de considerar es el valor de pH; no es una impureza o elemento, es sencillamente un valor numérico que representa el contenido potencial de hidrógeno del agua – que es una medida de acidez o alcalinidad del agua. El agua, H2O, tiene dos tipos de iones – iones de hidrógeno (H+) y iones de hidróxilo (OH-).
Si predominan los iones de hidrógeno, la solución será ácida con un valor de pH entre 0 y 6. Si predominan los iones de hidróxilo, la solución será alcalina, con un valor de pH entre 8 y 14. Si hay igual número de hidróxilo como iones de hidrógeno, entonces la solución será neutra, con un valor de pH de 7.
Los ácidos y alcalinos tienen el efecto de incrementar la conductividad del agua por encima de la de una muestra neutra. Por ejemplo, una muestra del agua con un valor 12 de pH tendrá una conductividad más alta que una muestra que tiene un valor 7 de pH.
Las siguientes tablas muestran los valores de pH como valores numéricos y su relación con sustancias de uso diario:

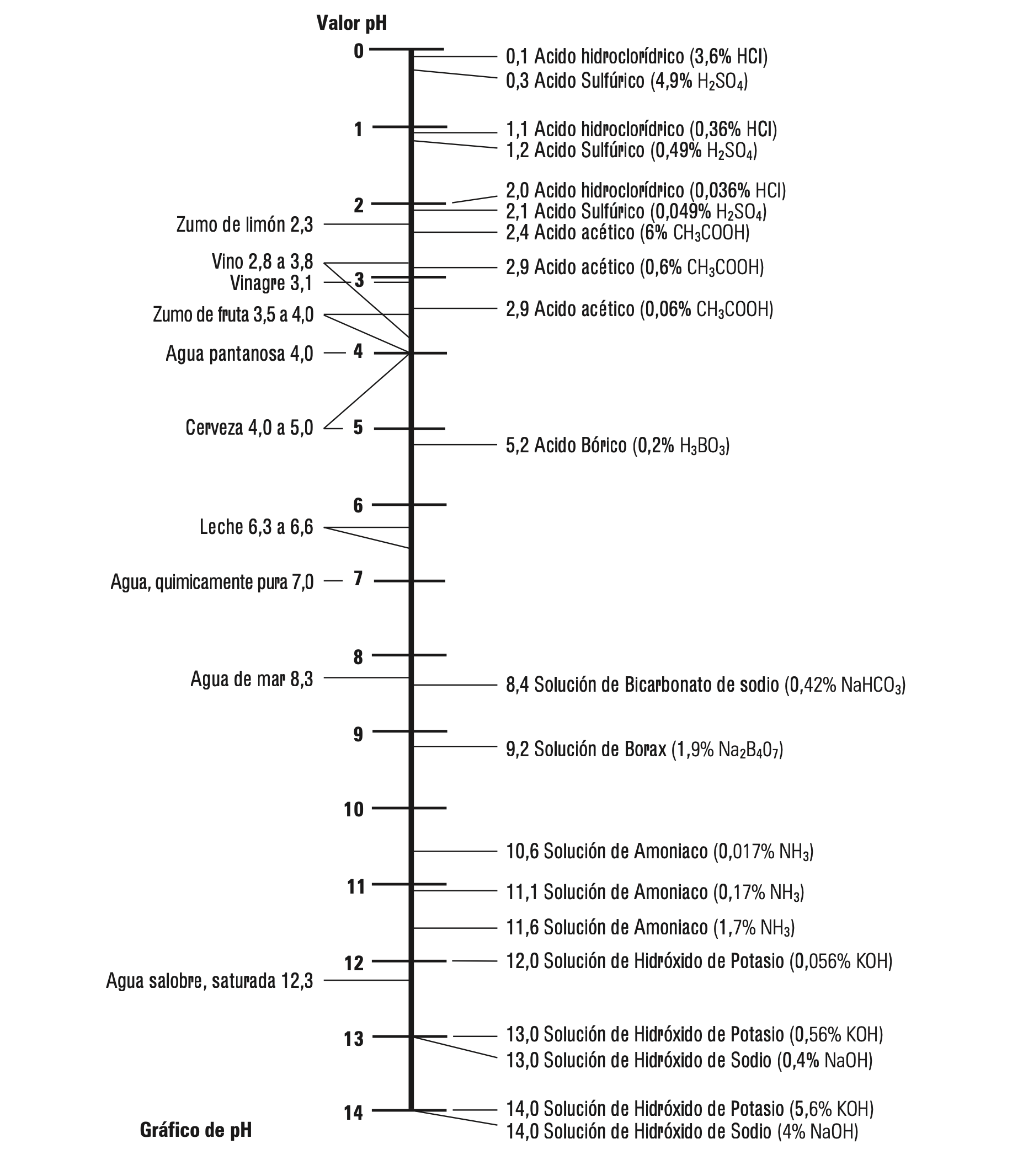
Ya que te interesa conocer más aspectos clave del tratamiento de agua para calderas de vapor, suscríbete al newsletter especializado en sistemas de vapor industrial, un recurso que te servirá para recibir más contenido sobre las nuevas tendencias del vapor, como lo que se debe tener en cuenta al momento de seleccionar un medidor de caudal para sistemas de vapor.



 Aspectos clave del tratamiento de agua para calderas de vapor
Aspectos clave del tratamiento de agua para calderas de vapor
Deja una respuesta